【JACS】1566倍的亮度跨越!中科大团队革新余辉成像技术,让深层肿瘤与帕金森病在“发光”中无所遁形
✨文章标题:Engineering Intermolecular Packing of Quinoid-Cyanine Scaffolds for Enhanced Afterglow Brightness and Activatable Imaging ✉️作者:Qingqing Miao* 等 🔗链接:https://doi.org/10.1021/jacs.6c01078
[!summary]
1. 研究背景与挑战
长余辉成像的优势: 与传统荧光成像相比,余辉成像在激发停止后发光,能够完美避开生物组织自带的“背景噪声”(自荧光),实现极高的灵敏度和深层组织穿透。
现有痛点: 传统的余辉探针通常需要多个组分混合,稳定性差且容易失效。虽然“自持续单分子余辉(SAMs)”简化了结构,但在制备成纳米颗粒时,分子间会发生严重的π-π堆积,导致聚集诱导猝灭(ACQ),大大降低了亮度和单线态氧的产生效率。
2. 核心创新方案
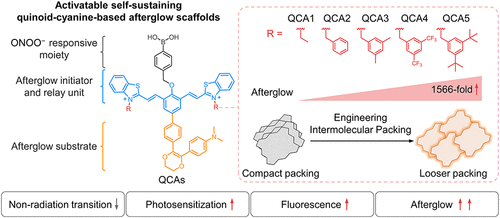
空间位阻策略: 研究团队设计了一系列醌式-花菁(Quinoid-Cyanine)骨架,命名为 QCAs (QCA1-QCA5)。其核心改动是在分子结构中引入不同大小的空间位阻基团(如叔丁基)。
堆积方式调节: 这种化学工程方法能够直接控制分子间的距离。从QCA1到QCA5,随着位阻增大,分子间的堆积由“紧密”变得“疏松”。
3. 关键性能数据
亮度飞跃: 优化后的 QCA5 纳米颗粒在 760 nm 处的余辉强度比基础款 QCA1 提高了惊人的 1566 倍。
机制解析: 理论研究和分子动力学模拟证实,疏松的堆积抑制了能量的非辐射衰减,同时增强了单线态氧的产生能力和荧光量子产率,三者合力造就了超高亮度。
4. 实际生物应用
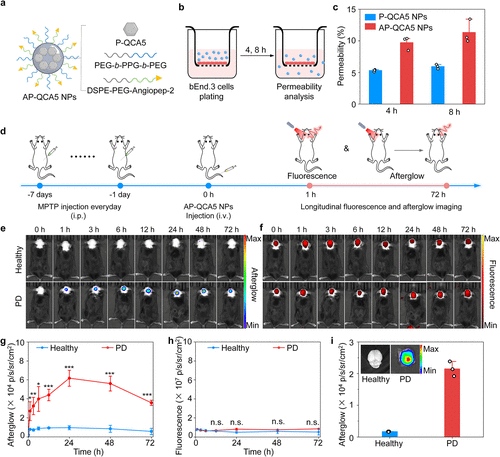
肿瘤特异性成像: 研究者利用过氧亚硝酸盐(ONOO⁻)响应的化学键“笼置”了 QCA5,开发出可激活探针 P-QCA5。在乳腺癌肿瘤模型中,该探针实现了高达 426 的信噪比(SBR)。
帕金森病(PD)早期诊断: 通过修饰能够穿透血脑屏障的肽链(Angiopep-2),探针成功检测到了 PD 小鼠脑部病理性的 ONOO⁻ 水平,成像对比度达到 6.5,而传统的荧光成像在此场景下几乎失效。
5. 研究意义
该研究提供了一套通用的化学工程框架,证明了通过调控分子间相互作用而非仅仅优化分子主链,可以大幅提升余辉性能,为开发下一代高灵敏、可激活的生物医学成像工具开辟了新路径。
一、 从“背景噪音”的痛点到深层成像的重大突破
在现代生物医学成像的宏伟版图中,科学家们始终在与一种看不见的“敌人”作斗争,那就是组织自荧光 。当我们尝试利用传统的荧光成像技术观察人体内部的病变时,外部激发光不仅会点亮我们投射的探针,还会不由自主地激发皮肤、脂肪和肌肉组织自带的荧光,这就如同在正午的烈日下寻找一只萤火虫,刺眼的背景杂讯极大地限制了成像的灵敏度和对比度 。为了打破这一僵局,分子余辉成像技术脱颖而出 。这种技术的神奇之处在于它能实现“光照停止,发光持续”,通过在时间轴上将激发过程与检测过程完全分离,它能够彻底消除组织自荧光的干扰,从而在极深的组织深度下捕捉到原本不可见的微弱信号 。
然而,早期的有机余辉探针往往依赖于复杂的“多组分混合”策略,需要将引发剂、底物和发光单元物理混合在一起 。这种笨重的设计不仅增加了系统的不确定性,还极易在复杂的生物环境中发生解体,导致功能失效 。虽然近年来科学界提出了自持续余辉分子(SAMs)的概念,尝试将所有功能集成到单一分子结构中,但新的问题接踵而至 。当这些分子被制备成便于在生物体内运输的纳米颗粒时,分子间会发生剧烈的π-π堆积,这种过于紧密的社交距离会引发严重的聚集诱导猝灭(ACQ)效应,使得探针的亮度在关键时刻大打折扣,甚至导致光敏化能力的全面溃败 。
针对这一制约行业发展的核心瓶颈,中国科学技术大学(USTC)团队在《美国化学会志》(JACS)上发表了颠覆性的研究成果 。他们并未选择传统的优化分子骨架的老路,而是另辟蹊径,提出了一套精妙的分子间堆积工程(Intermolecular Packing Engineering)策略 。通过在分子结构中引入不同级别的“空间位阻基团”,他们成功研发出了一系列具备自持续发光能力的醌式-花菁余辉骨架(QCAs) 。这一创新不仅将余辉强度推向了前所未有的 1566倍 增长,更为帕金森病(PD)和深层肿瘤的精准诊断开辟了全新的超高对比度成像路径 。
二、 核心方法与技术细节:打造分子的“社交距离”支架
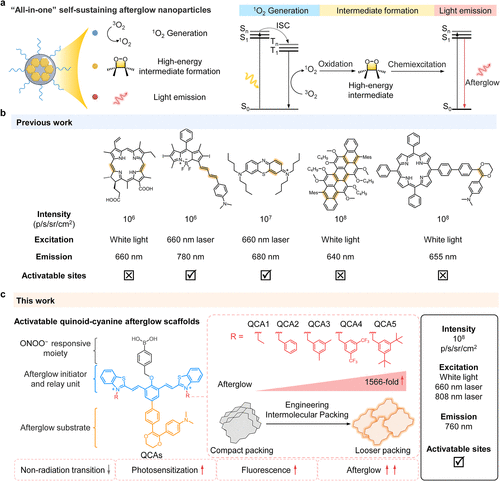
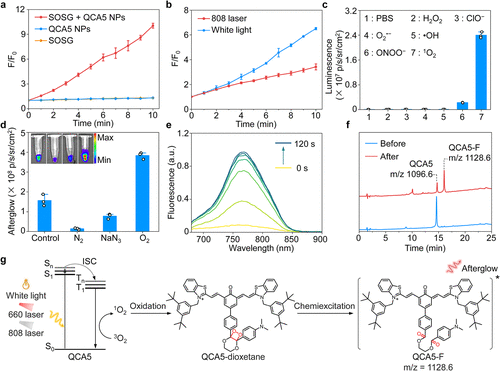
要理解这项研究的技术深度,我们必须深入到分子层面的精密构造之中。研究团队的核心任务是解决“自持续余辉分子在聚集态下变暗”的难题 。他们选用了醌式-花菁作为核心骨架,这一选择极具战略眼光 。在这种设计中,花菁单元扮演着双重角色:它既是捕捉能量的引发剂,也是最终释放光子的中继发光单元 。而与之相连的 N,N-二甲基-4-(3-苯基-5,6-二氢-1,4-二氧杂环己烯-2-基)苯胺(DO) 部分,则作为储存能量的余辉底物 。这种“全能型”的设计虽然简化了结构,但分子间的紧密堆积依然是发光效率的“杀手” 。
为了给分子撑开必要的“呼吸空间”,研究团队设计并合成了五种具有不同空间位阻的分子,命名为 QCA1 到 QCA5 。在分子的合成路径上,他们采用了极具逻辑性的化学手段。首先通过苏木基偶联(Suzuki coupling) 反应将羟基苯醛与 DO 部分连接,与此同时,制备了带有不同体积烷基链的苯并噻唑盐 。最后,通过经典的克内夫内格尔缩合(Knoevenagel condensation) 反应,将这些片段完美缝合在一起 。从 QCA1 到 QCA5,位阻基团的体积稳步增大,QCA5 更是装备了庞大的叔丁基结构 。这就像是在每个分子的四周安装了大小不一的“减震支架”,位阻越大的分子,其在聚集时的社交距离就保持得越好 。
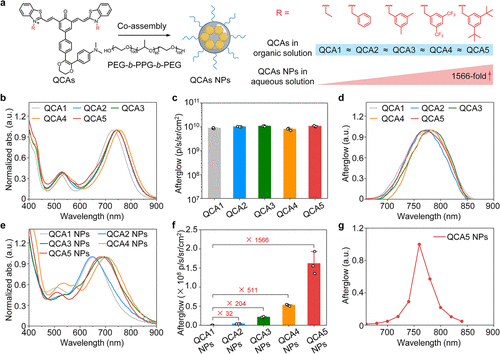
当这些疏水性的 QCAs 分子与两亲性共聚物 PEG-b-PPG-b-PEG 进行共组装后,便形成了直径约为 19.8 纳米 的水溶性纳米颗粒 。实验观测发现了一个极具启发性的现象:在有机溶剂中呈现分子分布状态时,QCA1 到 QCA5 的余辉表现相差无几,但在制备成纳米颗粒后,性能差距开始显现并迅速拉大 。研究团队通过紫外-可见吸收光谱观察到,纳米颗粒化后的分子表现出明显的蓝移,这证实了 H-聚集体的形成 。然而,QCA5 由于拥有最大的位阻基团,其分子间的堆积模式从 QCA1 的“密不透风”变成了“疏松有度”,这种堆积模式的工程化改变正是亮度飞跃的核心秘密 。
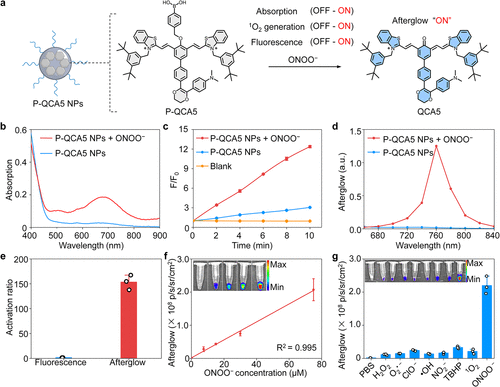
除了提升亮度,研究团队还为这一系统赋予了“智能开关”的功能 。他们利用醌式结构的天然可修饰性,引入了一个苯硼酸基团来封锁分子的电子共轭体系,开发出了针对过氧亚硝酸盐(ONOO⁻) 的激活型探针 P-QCA5 。在正常生理状态下,探针就像处于“休眠模式”,几乎不产生任何光信号 。但一旦遇到病理性的 ONOO⁻,分子的“笼子”就会被化学反应精准拆除,瞬间释放出具有强大发光能力的 QCA5 单元 。这种设计不仅进一步压低了背景信号,更让探针具备了识别特定病理过程的能力,从而在肿瘤微环境探测和神经疾病诊断中展现出极高的特异性 。
三、 数据背后的创新与颠覆性:从物理化学到生物成像的全面跨越
数据是科研成果最坚硬的骨架,而在团队的这项研究中,数据的对比展示了近乎“降维打击”式的性能优势。最令人震撼的数据莫过于 QCA5 纳米颗粒相比于 QCA1 实现了 1566 倍 的余辉强度增强 。这种跨越式的提升意味着,在同样的激光激发条件下,QCA5 产生的信号不仅肉眼清晰可见,更能在极深的生物组织中保持足够的穿透力 。这种亮度增强并非来自单一维度的优化,而是单线态氧产生能力与荧光量子产率共同提升的协同结果 。实验数据显示,经过氧化后的 QCA5-F 纳米颗粒,其荧光量子产率高达 23.9%,而基础款 QCA1-F 仅为 1.76%,这意味着能量在 QCA5 内部更多地转化为了光,而非无用的热能 。
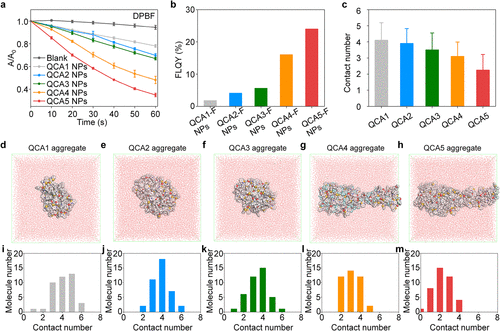
为了从分子动力学层面剖析这一现象,研究团队引入了精密的理论模拟 。他们通过计算定义了一个**“接触数”指标,用来量化分子之间的拥挤程度 。模拟结果清晰地显示,随着位阻基团的增大,分子间的平均接触数稳步下降,QCA5 的聚集体呈现出明显的“离散”特征 。这从物理层面证实了,位阻基团确实像“弹簧支架”一样撑开了分子间的距离,从而大幅降低了非辐射能量损耗,并极大地促进了光敏化路径**的效率 。这种对分子间相互作用的精准调控,相比于传统仅关注分子主链设计的思路,更具普适性和工程化的参考价值 。
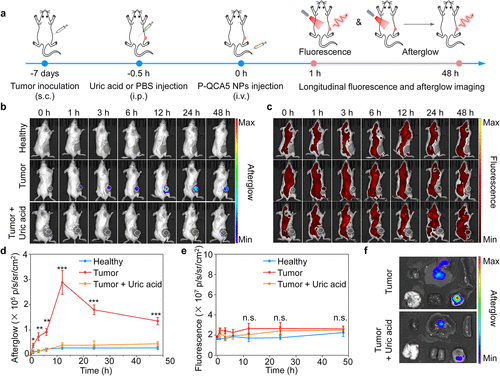
在肿瘤成像的实战演练中,激活型探针 P-QCA5 展现出了惊人的实战威力 。在 4T1 肿瘤模型小鼠的实验中,静脉注射探针 12 小时后,肿瘤区域的余辉信号达到了峰值,其信号背景比(SBR)竟然高达 426 。这一数值是健康对照组或预处理组的 5.9 倍到 8.4 倍之多 。最为关键的创新点在于对比:当研究人员尝试使用荧光成像观察同一组小鼠时,由于激发光的强烈干扰,荧光图像几乎无法分辨出肿瘤的边界,而余辉成像则像是一盏在黑暗中点亮的明灯,精准勾勒出了肿瘤的轮廓 。这种高达数百倍的信噪比提升,对于实现肿瘤的早期发现和手术中的边界确认具有不可估量的临床意义 。
然而,这项研究最具挑战性的应用场景在于大脑。帕金森病(PD) 的早期诊断一直是生物医学界的难题,其核心难点在于大脑有着严密的血脑屏障(BBB) 保护,且传统成像手段难以探测脑内微弱的病理标志物 。团队通过在探针表面修饰 angiopep-2 肽,成功赋予了探针跨越血脑屏障的能力,其渗透率相比未修饰前提升了 1.9 倍 。在 MPTP 诱导的帕金森病小鼠模型中,AP-QCA5 探针通过捕捉脑部过量的 ONOO⁻ 信号,实现了 6.5 的成像对比度 。这种清晰的差异在荧光成像下是完全无法观测到的 。这证明了高亮度、可激活的余辉探针不仅能看清肿瘤,更能深入人体的“禁区”大脑,捕捉到疾病初期的微弱火花 。
四、 应用展望、局限性与未来路线图:开启分子医学新篇章
中科大团队的这项研究不仅是一个化学合成的胜利,更是一场关于“分子秩序”的胜利。通过系统地调节空间位阻,他们证明了通过调控分子间相互作用而非单纯堆积能量,可以获得数量级级别的性能飞跃 。这种设计理念不仅适用于醌式-花菁体系,更可以作为一套通用的“化学工程框架”,指导未来更多自持续余辉材料的开发 。在未来的临床应用展望中,这种超亮探针有望成为精准外科手术导航的标配,帮助医生在术中实时识别人眼和传统成像设备难以发现的微小病灶 。
当然,作为一项处于科学前沿的探索,研究团队也客观地指出了现阶段的局限性 。目前余辉信号的半衰期大约在 1 分钟左右,虽然对于多次“充电”成像已经足够,但在某些需要极长时间连续观测的场景下,仍有待进一步提升发光时长 。此外,尽管探针在小鼠实验中表现出了良好的生物安全性和低毒性,但在进入人类临床试验之前,其在体内的长期代谢规律、潜在的免疫原性以及在不同人种间的响应一致性,仍需要大量且严谨的药代动力学研究来支撑 。
未来的路线图已经清晰地展现在我们面前。研究方向可能会向近红外二区(NIR-II, 1000-1700 nm)进一步延伸,利用更长的波长实现更深层的组织穿透和更高的分辨率 。同时,这种基于堆积工程的策略也可以与其他诊疗手段相结合,例如将高效率的单线态氧产生能力转化为光动力治疗(PDT) 的强大火力,实现“发现即治疗”的一体化诊疗方案 。总而言之,这项研究为我们揭示了一个真理:在分子的微观世界里,保持适当的“社交距离”不仅是一种生存智慧,更是释放巨大能量的关键钥匙 。